- Что обнаружил «фармвестник»
- «формакс» или «форлакс»
- Без гарантированного эффекта
- Защита прав потребителей — управление федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека по городу санкт-петербургу
- Как выбрать производителя бад? показатели качества.
- Какие законы нарушаются
- Каннабидиол (кбд, cbd)
- Клинические исследования лекарственных препаратов
- Лекарство от подделок
Что обнаружил «фармвестник»
В конце марта «ФВ» провел эксперимент и в рамках журналистского расследования приобрел пищевые добавки с веществами, запрещенными для использования в составе БАД. Некоторые из товаров, в основном для спортивного питания, были произведены в России.
В 2021-м и 2020 году «Фармвестник» проводил эксперимент с заказом доставки рецептурных препаратов без рецепта. Оба раза редакции привозили лекарства, в том числе психотропные, несмотря на то, что дистанционная торговля лекарствами на тот момент была запрещена. В 2020 году их привезли прямо в Минздрав. В этот раз «ФВ» решил закупить БАД, в составе которых есть запрещенные для использования вещества.
Так, на сайте IHerb была заказана добавка для спортивного питания Natrol 50 мг 50 таблеток. Она содержит дегидроэпиандростерон, он же — прастерон. В заказ вошла и биодобавка Gaia Herbs — одна жидкая унция (30 мл). Добавка содержит перец кава-кава, он же перец опьяняющий — Piper methysticum.
Несмотря на пандемию коронавируса, посылка была доставлена авиапочтой в Россию за неделю.
Также сотрудник «ФВ» приобрел на Wildberries экстракт ашвагандхы и якорцы стелющиеся на Беру.ру и ОZON. Эти вещества также запрещены для включения в состав БАД в соответствии с требованиями законодательства (Приложение 7 к техническому регламенту Таможенного союза «О безопасности пищевой продукции»).
«формакс» или «форлакс»
Роспотребнадзор уже направил в Евразийскую экономическую комиссию (ЕЭК) предложения внести изменения в техрегламент Таможенного союза «Пищевая продукция в части ее маркировки» (документ регулирует и БАДы), сообщили «Известиям» в ведомстве. Поправки предлагают запретить использовать в названиях биодобавок международные непатентованные наименования лекарств и зарегистрированные товарные знаки, под которыми производят медикаменты.
Мера коснется и наименований, сходных с ними до степени смешения, уточнили в Роспотребнадзоре. При этом критериев сходства будет три: семантический (смысловой), фонетический (звуковой) или транслитерационный (связанный с использованием для передачи названия другого алфавита).
Среди одноименных БАДов и лекарств, которые сейчас продаются в России, есть, например, «Глицин», «Аевит», «Ци-Клим», созвучные — БАД «Формакс» и лекарство «Форлакс», БАД «Энзим форте» и медикамент «Мезим форте», БАД «Сеалекс» и лекарство «Сиалис», похожие БАД «Фукус» и препарат «Фукус-плюс», БАД «Эректин-ЛАД» и лекарство «Эректин».
При покупке потребителю сложно ориентироваться, лекарство перед ним или биодобавка, пояснили в Роспотребнадзоре.
В ЕЭК подтвердили, что российская сторона уже определена разработчиком поправок касательно БАДов в «пищевой» техрегламент, и организация ведет консультации с Роспотребнадзором.
Если предложения будут приняты, пройдет ревизия реестра свидетельств о госрегистрации всех БАДов. По результатам этой работы Роспотребнадзор подготовит проект рекомендации Коллегии ЕЭК о принятии решения об изъятии из оборота биологически активных добавок, несоответствующих новым требованиям, сказали «Известиям» в пресс-службе ведомства.
Без гарантированного эффекта
В союзе производителей БАДов воздержались от комментариев. Оценить долю добавок, которые могут уйти с рынка, весьма проблематично, отметил генеральный директор маркетингового агентства DSM Group Сергей Шуляк. По его словам, сейчас по всем спорным случаям проводят экспертизу и судебное разбирательство. Тем не менее, по оценке эксперта, мера может затронуть до 20% наименований.
Запрет называть БАДы идентично лекарствам может привести к росту цен. Запрещенные препараты, скорее всего, выпустят под новыми брендами, предупредила глава Аптечной гильдии (некоммерческой отраслевой организации, созданной крупными фармацевтическими сетями) Елена Неволина.
Защита прав потребителей — управление федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека по городу санкт-петербургу
§
§
§
§
§
§
§
§
§
§
§
§
§
§
§
§
§
§
§
§
§
§
§
§
§
§
§
§
§
Как выбрать производителя бад? показатели качества.
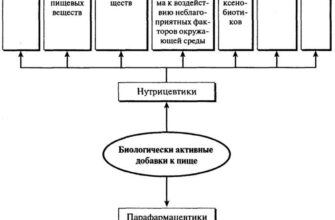
Проблемы здоровья современного человека связаны с загрязнением окружающей среды, стремительным ритмом жизни, нервным напряжением и, особенно, неправильным питанием. Дефицит микронутриентов ведёт к развитию хронических заболеваний и патологий, к раннему проявлению «возрастных» болезней, что доказано множеством исследований и признано авторитетными международными организациями. Включить биологически активные добавки к пище в ежедневный рацион значить начать укреплять защиту организма, повышать качество и продолжительность жизни. Сейчас приём биологически активных добавок стал необходимым и модным элементом образа жизни: многие звёзды и бьюти-блогеры делятся тем, какие БАДы для здоровья, энергии и красоты они принимают и результатами применения БАД. Актуальные вопросы, которые стоят перед потребителями: как сориентироваться в многообразии БАДов, какой БАД выбрать, где купить БАДы, которые будут качественными и эффективными? На какие параметры нужно обратить внимание и каким заявлениям производителей можно доверять?
Государственная регистрация БАД
В нашей стране каждая биологически активная добавка должна пройти государственную регистрацию, в ходе которой продукт проверяется на безопасность и содержание биологически активных веществ. Это делается в лабораторных условиях специальных сертифицированных центров. Контролем качества и регистрацией БАД занимается Роспотребнадзор. Поэтому первое, что нужно сделать, чтобы убедиться в безопасности БАД — проверить в реестре документов этой организации, зарегистрирована ли биологически активная добавка.
Добровольная сертификация БАД
БАД и лекарство – в чем их разница? В отличие от лекарственных средств, биологически активные добавки не подлежат обязательным клиническим испытаниям. То есть, доказывать их эффективность по закону — необязательно.
Но если все же производитель хочет убедиться и доказать потребителям, что действие БАДов на организм происходит должным образом и вызывает заявленный эффект — он может это сделать в рамках Системы добровольной сертификации биологически активных добавок к пище. Эту систему разработал «Центр гигиенического образования населения» Роспотребнадзора.
Для добровольной сертификации БАД привлекается третья независимая экспертная сторона, которая исследует, выясняет и предоставляет доказательства эффективности продукции. После чего, производитель имеет право информировать потребителя о полезных свойствах БАД на упаковке и в другой рекламе продукта.
Третьей независимой стороной выступает аккредитованная клиника, которая проводит клиническое исследование биодобавки.
Почему не все производители БАД подвергают свою продукцию клиническим испытаниям?
Казалось бы, доказанно эффективный бад (подтверждённый клинически) имеет конкурентное преимущество на рынке, а значит все производители должны быть заинтересованы в клинических испытаниях своих БАДов. Но проведение клинических испытаний – это сложный и дорогостоящий процесс. Не все клиники могут провести качественное исследование, так как эта работа требует высокой квалификации исследователей и соблюдения особых условий, а также достаточное количество подходящих для исследования пациентов. Аккредитованные клиники дорого ценят свои услуги. Если же в результате исследования БАД эффективность свою не докажет, то деньги на исследование будут потрачены впустую.
Поэтому далеко не все производители биологически активных добавок идут на такие дополнительные расходы и риски.
Что должно быть указано на упаковке качественного БАД?
-
Состав в порядке уменьшения весового или процентного содержания вещества
-
Свойства и способ применения, противопоказания
-
Слова «не является лекарством»
-
Срок годности и дата изготовления, условия хранения
-
Номер и дата госрегистрации
-
Информация о производителе с указанием контактов организации, которая принимает претензии от потребителей
-
Указание на сертификаты GMP (Good Manufacturing Practice – Надлежащая производственная практика) или ISO (международный стандарт качества производства, менеджмента и продукции)
Все этапы проверки качества и эффективности БАД Артлайф:

На начальных этапах разработки препаратов в лабораториях компании проводятся химические, физические, биологические, микробиологические, токсикологические и другие исследования. Эти проверки продукта помогают разработчикам повысить его качество, установить срок годности и условия хранения и выработать различные рекомендации для потребителей.
Следующий этап — это лабораторные исследования продукта в аккредитованном центре, который делает заключение о возможности обязательной сертификации БАД. Далее происходит сертификация и регистрация новой биодобавки в реестре Роспотребнадзора. После этой процедуры продукт готов к выходу на рынок.
Каждая новая партия продукции в процессе производства проходит дополнительные проверки в лабораториях Артлайф.
Практически все новые БАДы Артлайф отправляются на клинические исследования, иногда это происходит одновременно с выходом на рынок, а иногда не сразу, а после подтверждения востребованности продукта у потребителей. Исследование занимает в среднем 3-6 месяцев, после чего экспертами даётся заключение об эффективности БАДа и рекомендации приема. Эта информация размещается на упаковке, как реклама продукта (обоснованная и доказанная клинически).
Также вся информация, полученная в ходе клинических исследований, выносится на медицинские конференции, которые ежегодно проводит компания для своих партнеров.
После клинического исследования продукция проходит добровольную сертификацию и на ее упаковке появляется значок «КЛИНИЧЕСКИ ПОДТВЕРЖДЕНО»
Наталья Губина, начальник отдела регистрации и лицензирования Артлайф:
«Компания стремится охватить клиническими исследованиями весь ассортимент своих БАДов. Сегодня из 88 продуктов прошли клинику 57, то есть большая часть. Нужно отметить, что всегда в результате исследования подтверждается эффективность продукта и те его свойства, которые были заявлены изначально. Это говорит о высоком качестве наших разработок. Кроме того, исследования полезны тем, что часто спектр действия расширяется и мы получаем новые данные. Например, клинические исследования Олеопренов показали, кроме эффективности направленного действия, улучшение общего самочувствия, работоспособности, о чем свидетельствовали почти все участники исследования. Замечательно еще то, что по результатам исследования разработчики могут расширить и уточнить программы приема БАДа для его более продуктивного воздействия»
Почему Артлайф делает клинические исследования своей продукции?

Аккредитованные центры, с которыми мы сотрудничаем:
— Клиники СибГМУ (Сибирский государственный медицинский университет), г. Томск
— Городская клиническая больница №3 им. Б.И. Альперовича, г. Томск
—Томский НИИ курортологии и физиотерапии, г. Томск
Какие законы нарушаются
Продажа таких препаратов нарушает уже упомянутое 7-е приложение к техническому регламенту Таможен…
Каннабидиол (кбд, cbd)
Таблетки, леденцы, жвачки, крем, масло, капсулы, пластыри, жидкость для электронных сигарет и вейпа и так далее
Клинические исследования лекарственных препаратов
Для второй стадии клинических испытаний отбираются сотни человек со сходной патологией и без выявленных сопутствующих заболеваний. Различия по возрасту, полу, расе учитываются при формировании групп пациентов.
Набирая группу добровольцев, учёные стараются смоделировать заболевание в чистом виде. Пациенты должны иметь только интересующее исследователей заболевание. Тогда станет возможным оценить действие препарата по отношению к конкретному патологическому процессу.
Приоритетная задача
Данная фаза исследований не менее ответственна предыдущей. Безопасность лекарства доказана на здоровых людях. А какова будет реакция у человека с заболеванием?
Ставится новая задача — выявление безопасности и эффективности лекарственного средства на определённом контингенте больных.
Процесс
На данном этапе осуществляются исследования по подбору дозы препарата для достижения терапевтического эффекта: разовой, суточной, курсовой. Устанавливается кратность приёма. При испытании дозы многократно корректируются.
Также препарат должен доказать лечебный эффект в сравнении с плацебо (веществом, не имеющим активной субстанции).
Эффект плацебо состоит в том, что пациент может так понадеяться на лекарство, что самовнушение окажет положительное влияние на самочувствие, и результаты внушения ошибочно будут приняты за лекарственное воздействие. Вот почему помимо тестируемого препарата пациентам дают фиктивное лекарство (пустые таблетки, инъекции, мази).
Участники эксперимента подписывают документ, где соглашаются принимать препарат, не зная настоящий он или нет. Какой будет таблетка неизвестно даже врачу. Информацией владеет только организатор клинического исследования. Такой метод называется двойным слепым: о виде препарата не знает ни врач, ни пациент. Нужно исключить из анализа клинических испытаний субъективный фактор, способный исказить результаты.
Итог
Если эффективность и безопасность препарата на 2 фазе подтвердились, учёные получают разрешение на 3 стадию клинических исследований. До неё доходят единицы из заявленных лекарств.
Лекарство от подделок
Некоторые фармкомпании самостоятельно исключают появление «БАДов-подделок» на свои лекарства при регистрации брендов, рассказал управляющий партнер Экспертной группы Veta Илья Жарский. Роспатент регистрирует товарные знаки по классам товаров — одному или нескольким.
Эксперт привел пример: если компания А зарегистрирует бренд «Таблетка» только по пятому классу (лекарства), то компания Б может зарегистрировать то же самое наименование по 30-му классу (пищевые продукты, в том числе БАДы). Если же компания А подаст заявку на регистрацию товарного знака по обоим классам, то компании Б придется отказаться от своих планов.
— На практике крупные фармпроизводители подают заявки на регистрацию во всевозможные категории товаров, даже если у них нет никаких намерений всё это выпускать. Такой подход приводит к дополнительным расходам на уплату пошлин, зато позволяет избежать судебных издержек и нарушения собственных интересов в будущем, — пояснил Илья Жарский.
По данным DSM Group, в 2021-м розничный объем продаж БАДов в России составил 326 млн упаковок на сумму порядка 53,4 млрд рублей. За год рынок сократился на 0,6% в денежном и на 8,4% в натуральном выражении.